Compuestos iónicos
Propiedades principales
Estructura cristalina -> Forman redes sólidas y ordenadas de iones
Solubilidad en agua -> Muchos se disuelven fácilmente en agua
Conductividad eléctrica -> En solución o fundidos, conducen electricidad (los iones están libres)
Alto punto de fusión -> Se necesita mucha energía para romper las atracciones iónicas
Fragilidad -> Se rompen fácilmente si se golpean debido al desplazamiento de iones
Estructura iónica
Datos interesantes
-
La sal de mesa (NaCl) es un cristal cúbico perfecto y puede observarse con una lupa si se cristaliza lentamente.
-
Algunos compuestos iónicos como el nitrato de amonio (NH₄NO₃) son altamente explosivos si se calientan bruscamente.
-
Los electrolitos (como sales en agua) son compuestos iónicos y son esenciales para funciones nerviosas y musculares.
En el estado sólido, los compuestos iónicos forman una red tridimensional en la que cada ion positivo está rodeado de negativos y viceversa, maximizando la atracción y minimizando la repulsión.
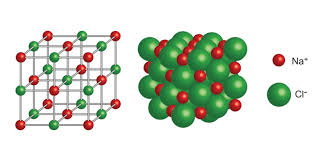

Índice de coordinación
Los distintos compuestos iónicos adoptan diferentes estructuras cristalinas características en las que los iones se colocan de forma peculiar en los nudos de la red. Las fuerzas atractivas y repulsivas se compensan.
Esta estructura debe cumplir dos condiciones:
• El empaquetamiento debe ser máximo: los iones deben ocupar el menor volumen posible.
• El cristal debe ser neutro: el número de cargas positivas ha de ser igual al de cargas negativas. Son de tamaño similar y cada uno de ellos puede ser rodeado por ocho iones de signo contrario.

El índice de coordinación o número de coordinación de un ion en una red cristalina iónica es el número de iones de signo contrario que le rodean a la misma distancia.
Para complementar mira el siguiente video